新闻中心
来源:米内网原创
总体承办情况:药品注册申请628个
据MED中国药品审评数据库2.0统计,2019年6月CDE共承办药品注册申请628个。除新增新药申请比上月有所上升外,仿制申请、进口申请以及补充申请(一致性评价)申请相比上月均有所回落。
2019年1-6月CDE承办药品注册申请情况(按受理号计)
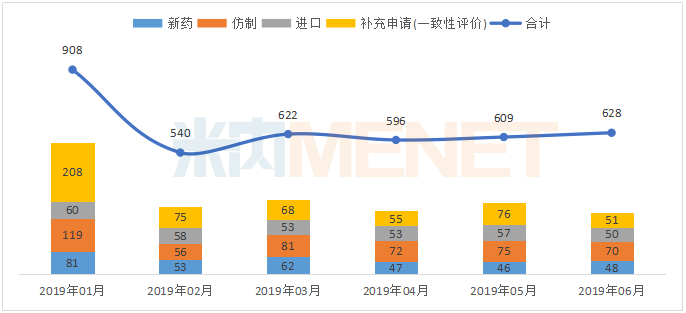
一致性评价承办情况:38个品种
6月有38个一致性评价品种获CDE承办(5月为59个),其中注射剂有10个。盐酸二甲双胍片目前已有6家企业通过仿制药一致性评价。
2019年6月CDE补充申请(一致性评价)品种承办情况
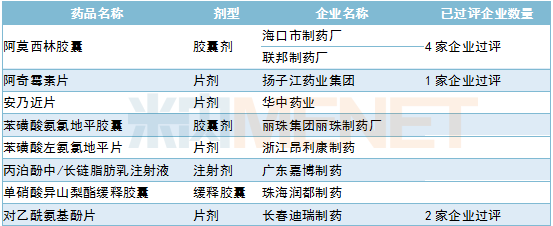
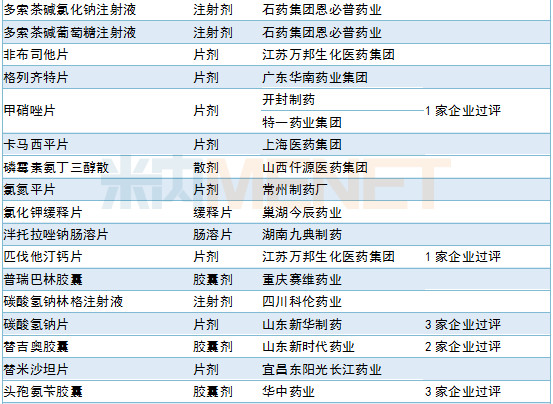
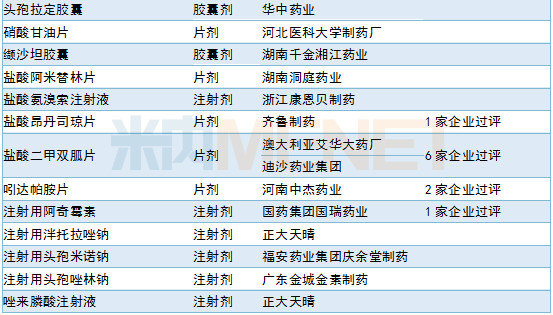
新药申请承办情况:27个新药
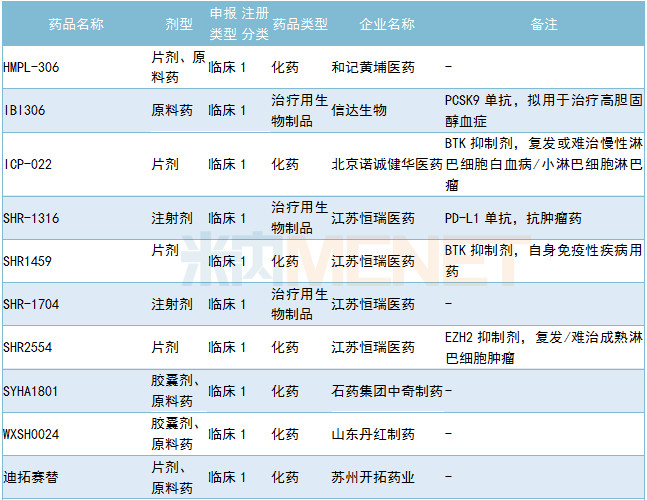
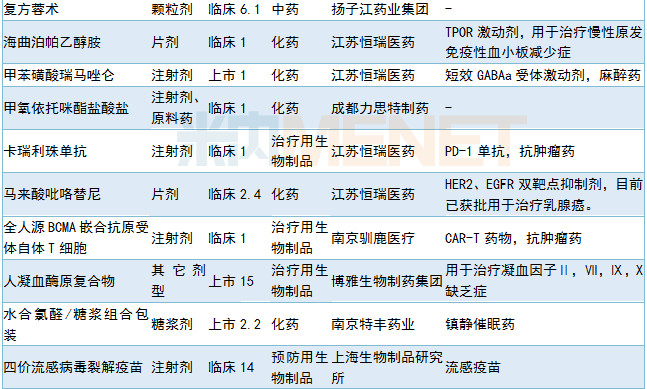
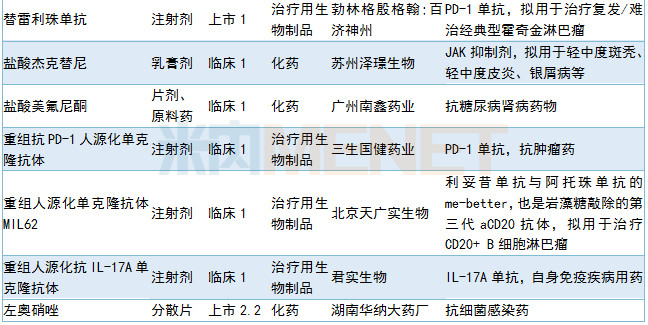
6月有27个新药获CDE承办,其中1类新药有21个。江苏恒瑞医药提交马来酸吡咯替尼新适应症临床申请,其他情况请见下表:
2019年6月国内新药申请承办情况
仿制申请承办情况:41个品种的仿制申请
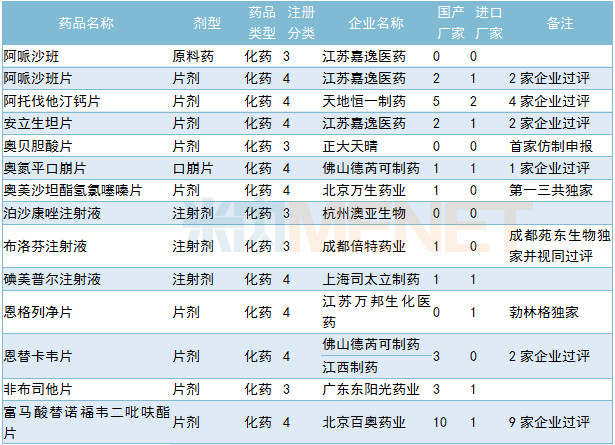
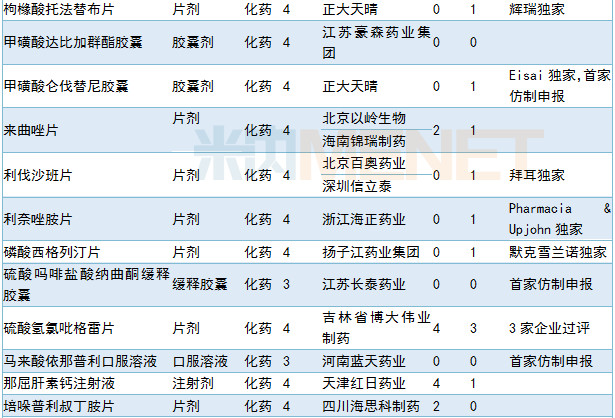
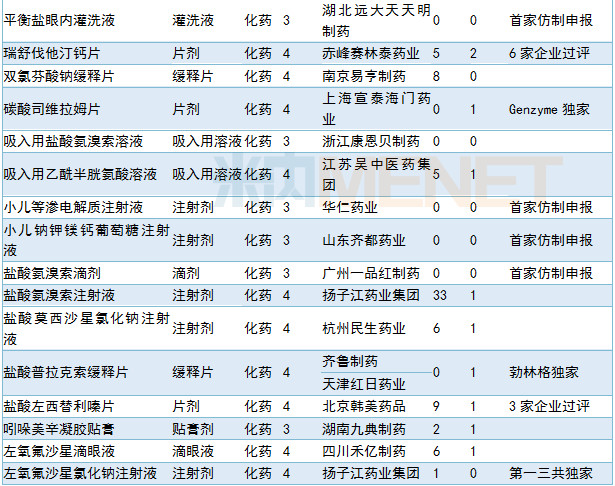
6月CDE共承办41个品种的仿制申请。有11个品种目前为国内独家品种,10个品种目前已有企业通过一致性评价。正大天晴首家提交奥贝胆酸片以及甲磺酸仑伐替尼胶囊仿制申请,其他情况请见下表:
2019年6月国产仿制申请承办情况
进口申请承办情况:33个品种的进口申请
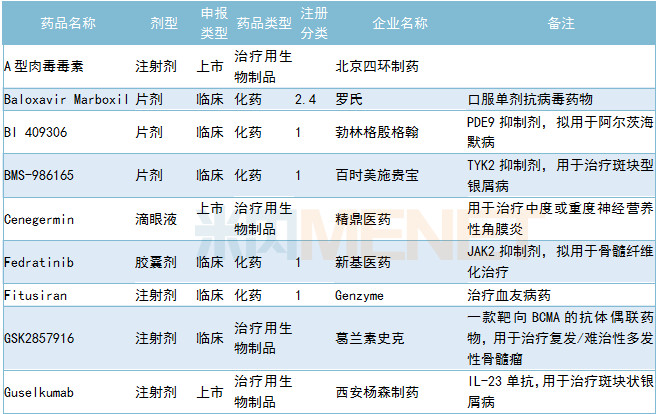
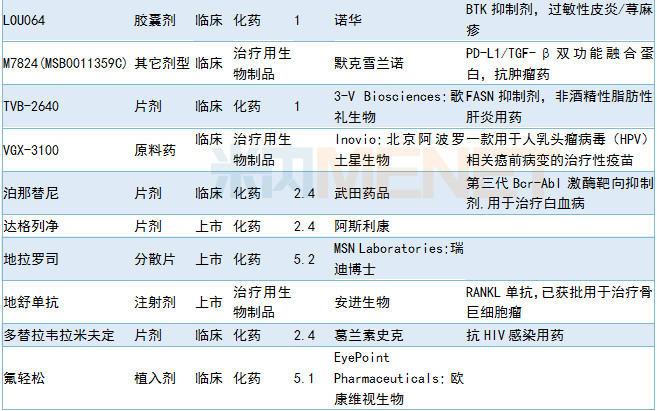
6月CDE共承办33个品种的进口申请,其中1类新药有6个,2.4类改良型新药、5.1类进口原研药以及5.2类进口仿制药各有5个。其他情况请见下表:
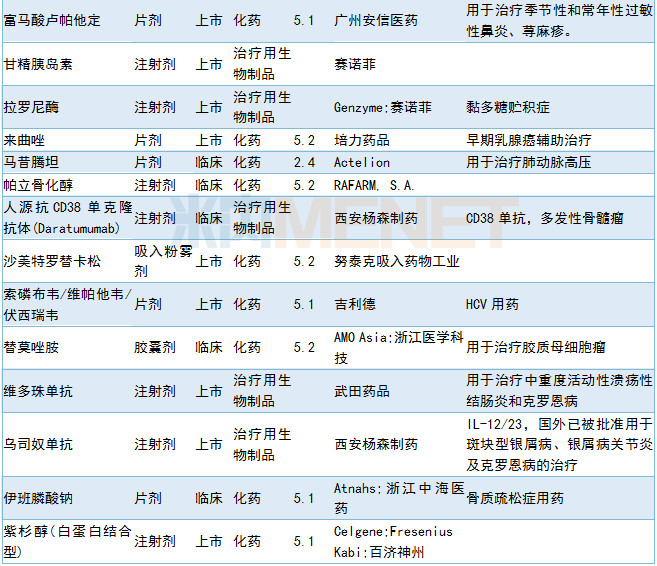
2019年6月进口申请承办情况
获批情况:9个品种过评,69个受理号获得临床试验默示许可
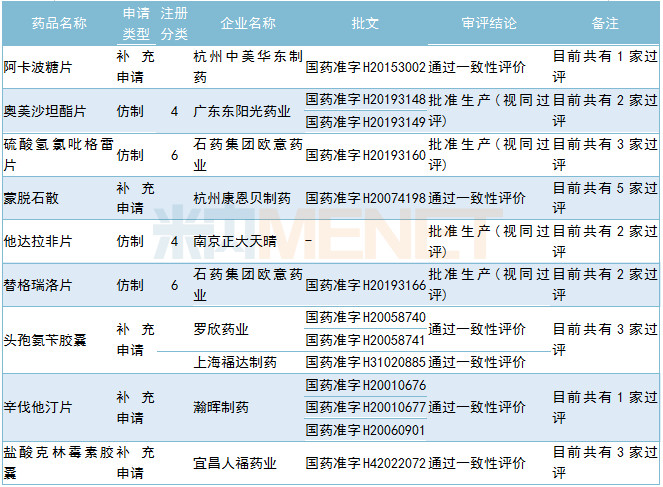
6月有9个品种(14个品规)通过或视同通过仿制药一致性评价,69个受理号获得临床试验默示许可。
2019年6月部分品种获批情况
2019年6月临床试验默示许可药品

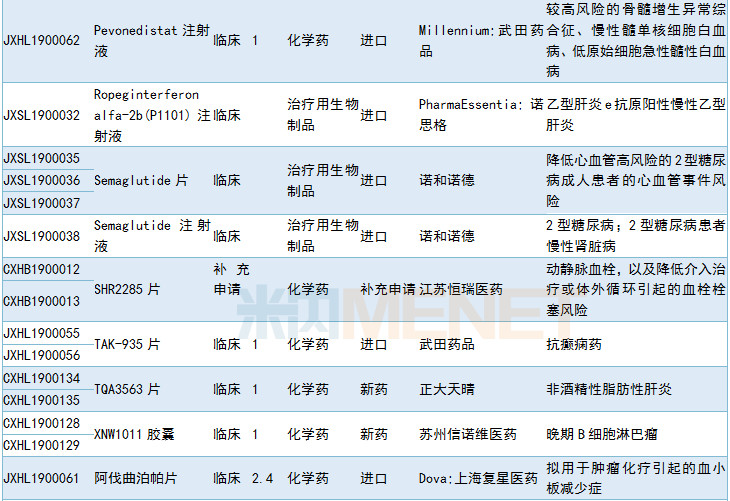
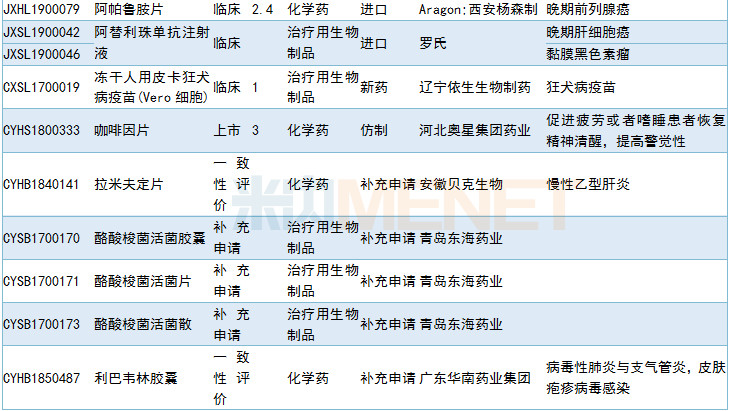

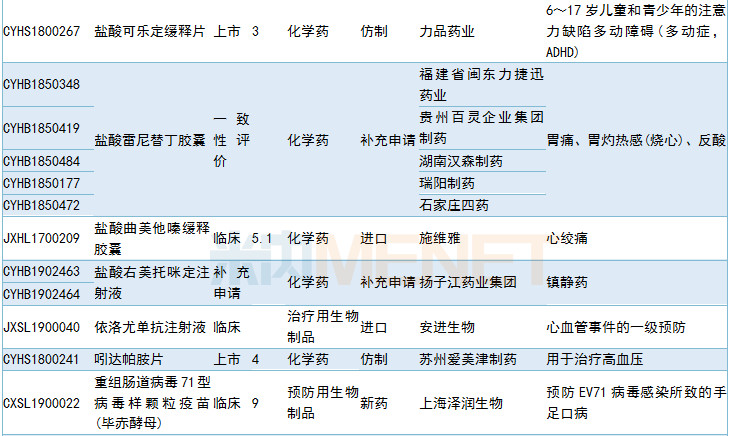
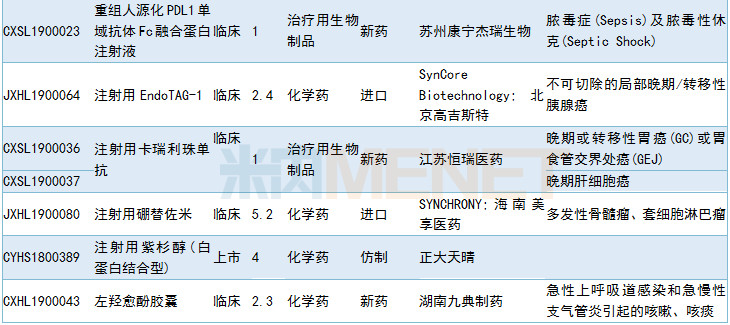
数据来源:米内网MED药品审评数据库2.0、CDE相关统计截至2019年7月2日,按药品名称统计
网站免责声明:
1.湖北海鸿医药有限公司对本网站上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。湖北海鸿医药有限公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
2.凡本网站注明"来源:XXX(非本网站)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网站赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网站发布,可与本网站联系,本网站视情况可立即将其撤除。
联系电话:027-84877900 邮件:1015566216@qq.com